Die Verbesserung von Herzunterstützungssystemen ist eine Anwendung, die uns buchstäblich am Herzen liegt. Ein Herzunterstützungssystem oder VAD („Ventricular Assist Device“) ist eine elektromechanische Pumpe zur Unterstützung des Herzkreislaufs, die dazu dient, die Funktion eines geschwächten oder ausfallenden Herzens teilweise zu ersetzen. VADs unterstützen entweder den rechten Ventrikel (RVAD), den linken Ventrikel (LVAD) oder beide Ventrikel (BiVAD).
Einige sind zur kurzfristigen Anwendung vorgesehen, typischerweise bei Patienten, die sich von einem Myokardinfarkt (Herzinfarkt) oder einer Herzoperation erholen, während andere zur Langzeitanwendung vorgesehen sind, typischerweise bei Patienten mit fortgeschrittener Herzinsuffizienz.
Normalerweise wird der Langzeit-VAD als Brücke zur Transplantation verwendet, um den Patienten in einem vernünftig guten Zustand am Leben zu halten und gleichzeitig die Herztransplantation außerhalb des Krankenhauses abwarten zu können. In einigen Fällen werden VADs jedoch auch als Zieltherapie verwendet, die eine Alternative zur Herztransplantation darstellt. Die Zieltherapie bietet langfristige Unterstützung bei Patienten, die nicht für eine Transplantation in Frage kommen.
Die in ventrikulären Unterstützungssystemen verwendeten Pumpen lassen sich in zwei Hauptkategorien einteilen: pulsierende Pumpen, die die natürliche Pulswirkung des Herzens nachahmen, und Pumpen mit kontinuierlichem Durchfluss. Pulsatile VADs verwenden Verdrängerpumpen. Kontinuierlich pumpende VADs sind kleiner und haben sich als langlebiger als pulsierende VADs erwiesen. Sie verwenden typischerweise entweder eine Kreisel- oder eine Axialpumpe.
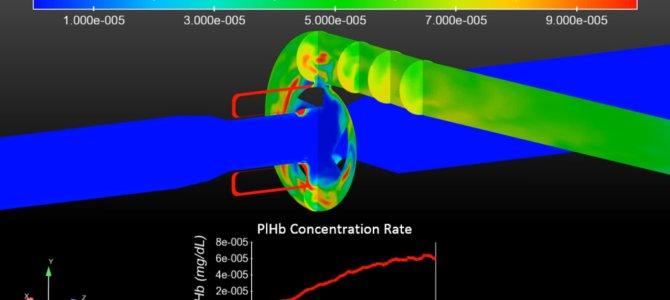
Thrombusbildung, erworbenes von-Willebrand-Syndrom und Hämolyse sind häufige unerwünschte Nebenwirkungen im Zusammenhang mit Herzunterstützungssystemen. Diese Ereignisse hängen in erster Linie von der Scherbeanspruchung, der Dehnungsrate und der turbulenten Energiedissipation im Fluid ab, die sich durch experimentelle Strömungsvisualisierung oder numerische Fluiddynamik (CFD) bestimmen lassen. Durch Optimieren der Komponenten des Geräts, z. B. der Rotor- und Gehäusegeometrien, können diese Eigenschaften so gesteuert werden, dass die oben genannten Nebenwirkungen minimiert werden.
Beispielfall: VAD Entwurf mit CONVERGE
Dieser Beispielfall ist Teil eines laufenden Projekts der Abteilung für Angewandte Biomedizinische Technik am Penn State College of Medicine. Gegenstand der Studie ist eine Kreiselpumpe zur Unterstützung des rechten Herzens (RVAD) und insbesondere – in diesem ersten Schritt – deren Laufrad. Ziel ist es, ein flexibles parametrisches Modell für das Laufrad in CAESES® zu erstellen, um schnell und einfach Varianten zu erstellen, die in Verbindung mit dem CFD-Löser CONVERGE zur Vorhersage von Pumpenkennlinien (HQ) oder für die CFD- getriebene Optimierung zur Reduzierung der turbulenten Energiedissipation (EPS) und Rezirkulationsbereiche in der Pumpe verwendet werden können.
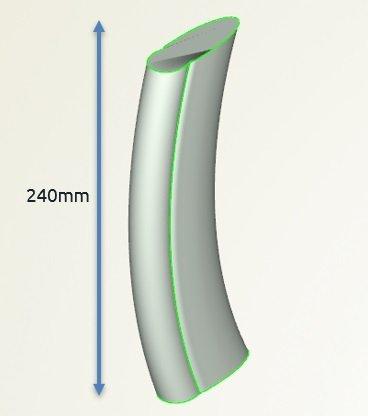
Die initiale Geometrie des Laufrads war zuvor in SOLIDWORKS entworfen worden und bestand aus einem für den Magnetantrieb erforderlichen torusförmigen Rotorkörper und drei geraden vertikalen Schaufeln. Während dieses einfache Design krude wirken mag, erwies es sich in Vorversuchen im Vergleich zu anderen möglichen Lösungen, wie beispielsweise profilförmigen Schaufeln, als relativ blutfreundlich.
Um diesen ursprünglichen Entwurf weiterzuentwickeln, wurde beschlossen, beim parametrischen CAESES®-Modell eine Verkleidung – im Grunde genommen einen Keil – auf der Saugseite der Schaufeln anzubringen. Die Saugseite ist von großem Interesse, da davon ausgegangen wird, dass sie sowohl die Größe und Form des Rezirkulationsgebiets hinter der Schaufel, als auch die Oberflächeneffekte auf der Rotoroberfläche bestimmt.
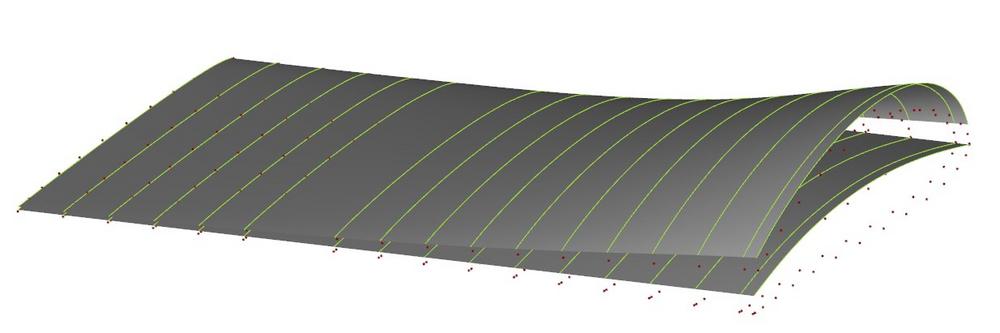
Die Innenfläche der saugseitigen Verkleidung ist mit einer B-Spline-Kurve modelliert, die eine flexible Formvariation unter Kontrolle einiger spezifischer Parameter ermöglicht. Zusätzliche Geometrieparameter steuern die Größe der Schaufeln in radialer und Umfangsrichtung, die Verrundungsradien an den Kanten der Geometrie und die Anzahl der Schaufeln.
Die Laufradgeometrie sowie andere Teile der Fluiddomäne der Pumpe, die zuvor in CAESES® importiert wurden, werden nach CONVERGE im proprietären, tessellierten Format „surface.dat“ exportiert, mit dem Oberflächenbereiche anhand ihrer Farbe und einer zugewiesenen ID identifiziert werden können. Dies ist erforderlich, um die Geometrie im Optimierungsprozess zu ersetzen, und dabei automatisiert die richtigen Randbedingungen zuweisen zu können. Darüber hinaus ermöglicht die Unterscheidung verschiedener Bereiche lokalere Vorhersagen von Werten wie EPS und Dehnungsrate.
Die Simulationssteuerung kann über CAESES® mithilfe der CONVERGE Eingabedateien im Software Connector verwaltet werden. Die Randbedingungen der Blutpumpe (wie Volumenstrom am Einlass, Auslassdruck und Rotordrehzahl), Simulationsparameter (wie Simulationsendzeit, Zeitschrittgrößen und Gittergröße) und Rechenleistung (die Anzahl der verwendeten Kerne) können alle in Parameter umgewandelt werden, sodass der Benutzer neue CONVERGE Simulationen manuell oder automatisch anpassen und ausführen kann, ohne die CONVERGE Oberfläche öffnen zu müssen.
Die Vorhersage der Pumpenleistung besteht aus der Erstellung von Kennlinien (Förderhöhe über Förderstrom, HQ) für eine bestimmte Pumpen- und Rotorkonfiguration. Für die Durchführung der HQ-Simulationen wird die Design Assembler Engine in CAESES® (in der der Benutzer bestimmte Wertekombinationen vorschreiben kann) verwendet, mit der mehrere Durchflussraten und Drehzahlen effizient automatisiert getestet werden können. Der Wirkungsgrad und der gemittelte EPS-Wert im Spiralgehäuse der Pumpe können zusammen mit den Standard-HQ-Kurven aufgezeichnet werden, um 3D-Diagramme zu erstellen, die eine umfassendere Leistungsbewertung ermöglichen.
Die Ergebnisse zeigen, dass die Funktion des Wirkungsgrads über HQ konvex ist und mindestens ein lokales, wenn nicht sogar globales Optimum für den Wirkungsgrad aufweist. Wenn mehr Bedingungen bei höheren Drehzahlen gefahren werden, könnte überprüft werden, ob der effizienteste Bereich bereits ermittelt wurde. Der gemittelte EPS-Wert weist eine positive Steigung vorwiegend in Drehzahl- und Delta-P-Richtung auf und ist daher von diesen Größen dominiert. Es besteht zwar auch eine Abhängigkeit von der Durchflussmenge, diese ist jedoch weniger stark ausgeprägt.
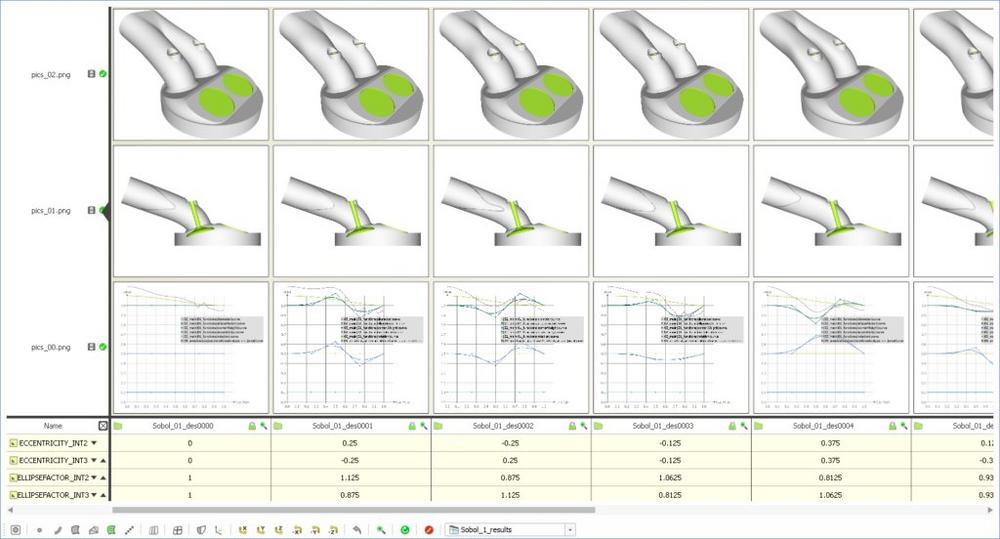
Explorative Studien zu den Designparametern des Rotors wurden sowohl mit dem Design Assembler als auch mit einem Latin Hypercube Sampling durchgeführt. Um mit begrenzten Ressourcen rechnerisch effizient zu sein, kann der Design Assembler verwendet werden, um zunächst größere Intervalle für die zu testenden Parameter festzulegen, bevor die Parameterbereiche verfeinert werden. Daran schließt sich ein DoE-Prozess (Design of Experiments) mit einer Latin Hypercube Sampling-Methode an, die eine genaue Sensitivitätsanalyse im verfeinerten Bereich der Designparameter liefert. Schließlich wird eine lokale Optimierung in einer vielversprechenden Region des Entwurfsraums gestartet, wie durch den vorherigen DoE-Prozess identifiziert.
Die aus den DoE-Studien gesammelten Daten haben die Korrelationen der berücksichtigten Rotorparameter mit dem EPS aufgedeckt, was dazu beitragen wird, zukünftige Optimierungen voranzutreiben. Hier schien die Länge der Verkleidung hinter den Schaufeln mit der gemittelten EPS-Wert den erkennbarsten Trend zu haben. Es wäre interessant, die Auswirkungen auf den EPS-Wert auf der Rotoroberfläche genauer zu untersuchen, da beide EPS-Werte in umgekehrter Beziehung zueinander zu stehen scheinen.
Die Ergebnisse aus der lokalen Optimierung deckten weiter die Auswirkungen der saugseitigen Geometrie auf EPS auf und zeigten den gleichen gut sichtbaren Zusammenhang zwischen der Verkleidungslänge und beiden EPS-Bewertungen. Weiterhin zeigte sich auch ein Zusammenhang mit dem Abstand der inneren Schaufelecke zum zentralen Loch des torusförmigen Rotorkörpers. Diese erste Optimierung wurde jedoch nur mit 10 Varianten durchgeführt, sodass diese Zusammenhänge verständlicher werden, sobald weitere Daten gesammelt werden.
Während die bisherigen Untersuchungen auf lokalen Ressourcen der Abteilung für Angewandte Biomedizinische Technik durchgeführt wurden, sollen künftige Studien an das Hochleistungsrechenzentrum des Penn State College of Medicine verlegt werden. Mit der Erhöhung der Rechenleistung sollen umfangreichere Optimierungen, einschließlich zusätzlicher Geometrievariablen, sowie teurere Auswertungen durchgeführt werden, die längere Rechenzeiten, feinere Rechengitter und LES-Berechnungen mit einem benutzerdefinierten EPS-basierten Hämolysemodell sowie ein auf der Dehnungsrate basierendes Modell für das Thrombusanfälligkeitspotential umfassen. Darüber hinaus werden weitere Komponenten des RVAD parametrisiert und in den Optimierungsstudien berücksichtigt, wie zum Beispiel das Spiralgehäuse.